У этого термина существуют и другие значения, см. Карбонаты (значения).Не следует путать с Карбонадом — продуктом из мяса.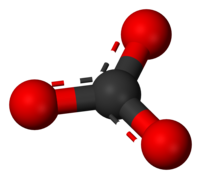 Модель карбоната иона
Модель карбоната иона
Карбона́ты и ги́дрокарбонаты — соли и эфиры угольной кислоты (H2CO3). Среди солей известны нормальные карбонаты (с анионом СО32−) и кислые или гидрокарбонаты (с анионом НСО3−).
Растворимость
Из нормальных карбонатов в воде растворимы только соли щелочных металлов, аммония и таллия. Вследствие гидролиза растворы их показывают щелочную реакцию. Малорастворимы нормальные карбонаты кальция, бария, стронция и свинца. Все кислые карбонаты хорошо растворимы в воде; кислые карбонаты сильных щелочей также имеют слабощелочную реакцию.
Химические свойства
- При нагревании кислые карбонаты переходят в нормальные карбонаты:
- 2NaHCO3⟶Na2CO3+H2O+CO2↑{displaystyle {mathsf {2NaHCO_{3}longrightarrow Na_{2}CO_{3}+H_{2}O+CO_{2}uparrow }}}
- При сильном нагревании нерастворимые карбонаты разлагаются на оксиды и углекислый газ:
- CaCO3⟶CaO+CO2↑{displaystyle {mathsf {CaCO_{3}longrightarrow CaO+CO_{2}uparrow }}}
- Карбонаты реагируют с кислотами сильнее угольной (почти все известные кислоты, включая органические) с выделением углекислого газа, эти реакции являются качественными реакциями на наличие карбонатов в растворе[1]:
- Na2CO3+2HCl⟶2NaCl+H2O+CO2↑{displaystyle {mathsf {Na_{2}CO_{3}+2HCllongrightarrow 2NaCl+H_{2}O+CO_{2}uparrow }}}
- NaHCO3+HCl⟶NaCl+H2O+CO2↑{displaystyle {mathsf {NaHCO_{3}+HCllongrightarrow NaCl+H_{2}O+CO_{2}uparrow }}}
Распространение в природе
Нормальные карбонаты широко распространены в природе, например: кальцит СаСО3, доломит CaMg(CO3)2, магнезит MgCO3, сидерит FeCO3, витерит ВаСО3, баритокальцит BaCa(CO3)2 и др. Существуют и минералы, представляющие собой основные карбонаты, например, малахит CuCO3·Cu(ОН)2.
Гидрокарбонаты натрия, кальция и магния встречаются в растворённом виде в минеральных водах, а также, в небольшой концентрации, во всех природных водах, кроме атмосферных осадков и ледников. Гидрокарбонаты кальция и магния обуславливают так называемую временную жёсткость воды. При сильном нагревании воды (выше 60 °C) гидрокарбонаты кальция и магния разлагаются на углекислый газ и малорастворимые карбонаты, которые выпадают в осадок на нагревательных элементах, дне и стенках посуды, внутренних поверхностях баков, бойлеров, труб, запорной арматуры и т. д., образуя накипь.
Применение
Карбонаты кальция, магния, бария и др. применяют в строительном деле, в химической промышленности, оптике и др. В технике, промышленности и быту широко применяется сода (Na2CO3 и NaHCO3): при производстве стекла, мыла, бумаги, как моющее средство, при заправке огнетушителей, в кондитерском деле. Кислые карбонаты выполняют важную физиологическую роль, являясь составной частью буферных систем крови, поддерживающих постоянство её рН.
Карбонаты органические
Сложные эфиры угольной кислоты. Средние ациклические карбонаты — бесцветные жидкости с эфирным запахом; не растворимы или труднорастворимы в воде, этаноле, диэтиламине, аммиаке, растворяются в эфире, ацетоне, бутиламине, бензиламине; образуют азеотропные смеси с водой, спиртами, тетрахлорметаном, этиленхлоргидрином, гексаном, циклогексаном. Циклические — жидкие или легкоплавкие твёрдые вещества; растворяются в воде, смешиваются с ароматическими углеводородами, спиртами, карбоновыми кислотами, ацетоном, хлороформом; не растворимы в алифатических углеводородах, сероводороде; образуют азеотропные смеси с гликолями. Наиболее употребителен диметилкарбонат (см. Карбонилирование)[2].
Литература
- Химия 9. — М.: Вентана-Граф, 2010. — С. 287.
Примечания
- ↑ Ходаков Ю. В., Эпштейн Д. А., Глориозов П. А. § 8. Реакции ионного обмена // Неорганическая химия. Учебник для 9 класса. — 7-е изд. — М: Просвещение, 1976. — С. 15—18. — 2 350 000 экз.
- ↑ Химия 9. — М.: Вентана-Граф, 2010. — С. 287.
