Нетрансли́руемые о́бласти (НТО, англ. untranslated regions, UTR) — особые участки мРНК, не выступающие в качестве матрицы для синтеза белка и прилегающие с обеих сторон к транслируемой области (то есть той, на матрице которой синтезируется белок). Таких области две: 5′-нетранслируемая область, или 5′-НТО (англ. 5′-untranslated region, 5′ UTR) и 3′-нетранслируемая область, или 3′-НТО (англ. 3′-untranslated region, 3′ UTR), располагающиеся на 5′- и 3′-конце мРНК соответственно[1]. Такое же название имеют участки ДНК, соответствующие 5′-UTR и 3′-UTR транскрипта[2].
Нетранслируемые области вовлечены в регуляцию локализации, трансляции, и деградации того транскрипта, в составе которого они находятся. Для них характерно наличие шпилек, внутренних инициаторных кодонов и открытых рамок считывания, сайтов связывания рибосомы, различных цис-регуляторных элементов, связывающихся с РНК-связывающими белками[3]. Так, в них локализованы такие элементы, как IRES, uORF, ARE[3], последовательность Шайна — Дальгарно, рибопереключатель и другие[4].
Содержание
- 1 Структурные особенности
- 2 Функции
- 3 UTR прокариот и вирусов
- 4 Клиническое значение
- 5 Примечания
- 6 Литература
- 7 Ссылки
Структурные особенности
 Шпильки во вторичной структуре 5′-UTR и 3′-UTR
Шпильки во вторичной структуре 5′-UTR и 3′-UTR
Анализ геномов различных организмов показал наличие ряда консервативных свойств, присущих нетранслируемым областям. Общая длина 5′-UTR приблизительно одинакова среди всех таксономических групп эукариот и составляет от 100 до 200 нуклеотидов (впрочем, у дрожжей Schizosaccharomyces pombe длина 5′-UTR в транскрипте ste11 составляет 2273 нуклеотида[5]). В то же время длина 3′-UTR гораздо более вариабельна и может составлять от 200 нуклеотидов у растений и некоторых животных до 800 нуклеотидов у человека и других позвоночных. Поразительным является тот факт, что длина как 5′-, так и 3′-UTR значительно изменяется в пределах одного вида, она может принимать значение от 12 до нескольких тысяч нуклеотидов[6]. Действительно, в in vitro системе, моделирующей генетический аппарат млекопитающих, показано, что даже 5′-UTR длиной в 1 нуклеотид может обеспечивать нормальную инициацию трансляции[7].
Участок геномной ДНК, соответствующий нетранслируемым областям мРНК, может содержать интроны, причём чаще в области 5′, чем в 3′. Около 30 % генов Metazoa имеют участки, соответствующие 5′-UTR, состоящие только из экзонов, в то же время в 3′-UTR, хотя она и длиннее, интронов гораздо меньше. Общая доля интронных последовательностей в 3′-UTR составляет 1—11 %. Образование альтернативных нетранслируемых участков имеет место при использовании различных сайтов начала транскрипции, сайтов полиаденилирования и сплайсинга. Для таких альтернативных нетранслируемых областей показана изменчивость их количества в зависимости от ткани, стадии развития, наличия болезненного состояния, они могут значительно влиять на экспрессию тех или иных генов[8].
Состав оснований также различается в 3′- и 5′-UTR, так, например, в 5′-UTR выше содержание G+C, чем в 3′-UTR. Особенно это различие заметно в мРНК теплокровных позвоночных, у которых содержание G+C в 5′-UTR составляет 60 %, а в 3′-UTR — 45 %[9]. Существует также определённая связь между содержанием G+C в 5′-UTR и 3′-UTR и третьими позициями в кодонах соответствующей транслируемой области. Также обнаружена важная обратная связь между содержанием G+C в 5′-UTR и 3′-UTR и их длинами[10]. В частности, известно, что гены, локализованные в GC-богатых участках хромосом (тяжёлые изохоры), имеют более короткие 5′-UTR и 3′-UTR, чем гены, расположенные в изохорах, более бедных GC. Похожая связь была показана для кодирующих последовательностей и интронов[11].
Наконец, в нетранслируемых областях мРНК эукариот было установлено наличие повторяющихся последовательностей различных типов, например, SINEs (в том числе Alu-повторов) и LINEs, минисателлитов и микросателлитов. У человека повторы мРНК составляют 12 % 5′-UTR и 36 % 3′-UTR, в других таксонах, в том числе у других млекопитающих, было показано меньшее содержание повторов[3].
Функции
Нетранслируемые области выполняют ключевые функции в посттранскрипционной регуляции экспрессии генов, включая модуляцию транспорта мРНК из ядра, регуляцию внутриклеточной локализации мРНК[12], её стабильности[13] и эффективность трансляции[14]. Нетранслируемые области могут играть роль и в других процессах, например, в котрансляционном включении нестандартной аминокислоты селеноцистеина по кодону UGA (обычно это стоп-кодон) мРНК, кодирующих селенопротеины (в этом процессе участвует консервативная шпилька, расположенная в 3′-UTR — SECIS-элемент)[15]. Важность нетранслируемых областей в регуляции экспрессии генов подтверждается ещё и тем, что мутации, затрагивающие эти области, могут приводить к серьёзным патологиям[16] (подробнее о заболеваниях, обусловленных мутациями в UTR, см. ниже).
Регуляция, осуществляемая нетранслируемыми участками мРНК, может быть опосредована несколькими путями. Нуклеотидные мотивы, расположенные в 3′-UTR и 5′-UTR, могут взаимодействовать со специфическими РНК-связывающими белками. В отличие от регуляторных элементов, локализованных в ДНК, у которых ведущую роль играет первичная структура ДНК (то есть последовательность нуклеотидов), биологическая активность регуляторных мотивов, расположенных на РНК, определяется и их первичной, и вторичной структурой. Также ключевые роли в регуляции были показаны для взаимодействий между участками нетранслируемых областей и специфическими комплементарными некодирующими РНК, в частности, микроРНК[17]. Наконец, известны примеры повторяющихся элементов, важных для регуляции экспрессии генов на уровне РНК, например, CUG-связывающие белки могут взаимодействовать с CUG-повторами в 5′-UTR специфической мРНК (например, кодирующей транскрипционный фактор C/EBPβ) и тем самым влиять на эффективность трансляции[18].
Контроль эффективности трансляции
Эффективность трансляции мРНК может быть различной, поэтому возможна регуляция количества получающегося белка. Это является важным механизмом регуляции экспрессии гена. Действительно, лишь для секретируемых белков существует чёткая связь между количеством мРНК и белка (чем больше мРНК, тем больше белка). У белков, предназначенных для внутриклеточного использования, эта взаимосвязь в значительной мере искажается различными темпами трансляции различных мРНК[19].
Структурные особенности 5′-UTR имеют важное значение для контроля трансляции. Показано, что мРНК, кодирующие белки, участвующие в процессах развития, например, факторы роста, транскрипционные факторы или продукты протоонкогенов (белки, для которых необходим чёткий контроль экспрессии), имеют 5′-UTR длиннее среднего[20], содержащие внутри инициаторные кодоны (англ. upstream initiation codons) и открытые рамки считывания, а также стабильные элементы вторичной структуры, препятствующие процессу трансляции (например, квадруплексы). Другие специфические мотивы и элементы вторичной структуры 5′-UTR могут модулировать эффективность трансляции[3].
В норме после перемещения мРНК из ядра в цитоплазму в области кэпа, расположенном на 5′-конце мРНК, собирается белковый комплекс eIF4F. В этот комплекс входят 3 субъединицы: eIF4Е (кэп-связывающий белок); eIF4А, обладающий хеликазной активностью; eIF4G, взаимодействующий с различными другими белками, в том числе с полиаденилат-связывающим белком. АТФ-зависимая хеликазная активность eIF4А, стимулируемая РНК-связывающим белком eIF4B, обеспечивает расплетание любых элементов вторичной структуры мРНК, в результате чего образуется «площадка для посадки» малой (40S) субъединицы рибосомы[21]. Если трансляцию сдерживает количество рибосом или концентрация факторов трансляции, 3′-поли(А)-хвост может взаимодействовать с 5′-кэпом, усиливая инициацию трансляции путём внедрения полиаденилат-связывающего белка, который может взаимодействовать с комплексом eIF4F[22].
Считается, что в эукариотических мРНК трансляция начинается с первого кодона AUG (стартовый кодон), который встретится рибосоме на её пути от 5′- к 3′-концу. Последовательности, окружающие стартовые кодоны, неслучайны и составляют консенсусную последовательность Козак. У млекопитающих эта последовательность имеет следующий вид: GCCRCCaugG, и наиболее консервативными нуклеотидами являются R (пурин, обычно А) на позиции −3 относительно AUG и G в позиции +4 относительно AUG. Строгое расположение А в позиции −3 и G в позиции +4 также характерно для других животных, растений и грибов. Последовательности, составляющие окружение AUG (частично они заходят в нетранслируемую область), могут модулировать эффективность трансляции, обеспечивая подходящее окружение для инициации[3].
Следует отметить, что от 15 % до 50 % 5′-UTR содержат внутри стартовый кодон AUG. Поэтому правило, согласно которому рибосома начинает трансляцию с первого стартового кодона, который встретится ей при перемещении от 5′- к 3′-концу мРНК, выполняется далеко не всегда. Это означает, что иногда рибосома может пропускать встречающиеся ей триплеты AUG и начинать трансляцию с более удалённого стартового кодона, возможно из-за того, что эти триплеты имеют «слабое» нуклеотидное окружение. Таким образом, с одной мРНК может быть синтезировано несколько различных белков[23]. Более того, установлено, что наличие внутренних кодонов AUG в 5′-UTR коррелирует с увеличенной длиной этой области и более «слабым» окружением обычно используемого стартового кодона, а в транскриптах с оптимальным окружением стартового AUG 5′-нетранслируемая область короткая и не содержит AUG[24]. В связи с этим AUG в 5′-UTR могут уменьшать уровень трансляции своей мРНК.
Если в 5′-UTR после внутреннего AUG, но перед основным стартовым кодоном располагается внутренний стоп-кодон, то образуется открытая рамка считывания (англ. upstream open reading frame, uORF). После трансляции uORF и диссоциации от мРНК большой (60S) субъединицы рибосомы, судьба малой субъединицы может быть различной, и это может оказать влияние на эффективность трансляции и стабильность мРНК. Малая субъединица может остаться на мРНК, возобновить считывание и начать трансляцию с нижележащего кодона AUG, а может покинуть мРНК и тем самым понизить уровень трансляции основной открытой рамки считывания. У эукариот способность рибосомы к возобновлению трансляции ограничивается, во-первых, стоп-кодонами[25] и, во-вторых, длиной uORF: если длина uORF превышает 30 кодонов[26], рибосома не сможет возобновить трансляцию. Таким способом блокируется трансляция мРНК, содержащих uORF, кодирующих транскрипционные факторы дрожжей GCN4 и YAP1[27].
Важное значение в регуляции трансляции имеет вторичная структура 5′-UTR. Экспериментальные данные показывают, что умеренно стабильные элементы вторичной структуры (значение изменения свободной энергии ΔG выше −30 ккал/моль), непосредственно содержащие стартовый кодон AUG, не останавливают малую субъединицу рибосомы. Существенное влияние на эффективность трансляции оказывают очень стабильные структуры (ΔG ниже −50 ккал/моль), снижая её. Преодолению влияния таких структур способствует повышение концентрации eIF4A[28].
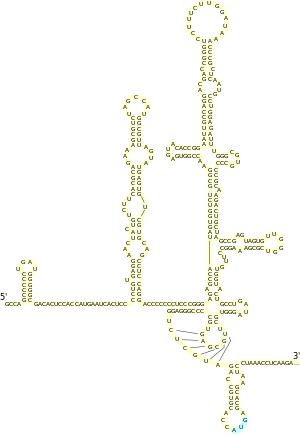 Строение элемента IRES вируса гепатита С
Строение элемента IRES вируса гепатита С
Существует альтернативный механизм инициации трансляции, не связанный с 5′-кэпом. Впервые он был описан у пикорнавирусов[29]. В этом случае внутри 5′-UTR существует особая последовательность, служащая для связывания рибосомы — IRES. В дальнейшем IRES были обнаружены во многих клеточных мРНК, кодирующих регуляторные белки, например, продукты протоонкогена c-Myc, гомеодоменные белки, факторы роста (например, фактор роста фибробластов FGF2[en]), а также рецепторы к ним[3]. Сравнительный анализ известных клеточных IRES позволил выделить общий структурный мотив, характерный для содержащих их мРНК. В частности, для мРНК белка, связывающегося с тяжёлой цепью иммуноглобулина (BiP), и мРНК белка FGF-2 была описана Y-образная шпилька, расположенная непосредственно перед стартовым кодоном AUG[30]. Установлено, что короткие структурные мотивы[en], комплементарные малым рибосомным РНК, могут также выступать как IRES[31].
Последовательности, являющиеся мишенями транс-функционирующих РНК-связывающих белков, могут также принимать участие в регуляции трансляции. Например, железозависимый элемент IRE (англ. iron-responsive element), локализованный в 5′-UTR мРНК, кодирующих белки, вовлечённые в метаболизм железа (ферритин, 5-аминолевулинатсинтаза[en] и аконитаза?!), может блокировать трансляцию. При этом происходит железозависимое связывание белков метаболизма железа, подавляющее нормальное сканирование мРНК, осуществляемое малой субъединицей рибосомы при инициации трансляции. Наконец, в большей части мРНК позвоночных, кодирующих рибосомные белки и факторы элонгации трансляции, содержится 5′-терминальный пиримидиновый тракт (англ. terminal oligopyrimidine tract (TOP)), непосредственно прилегающий к кэпу. Этот тракт необходим для координированной репресии трансляции в ходе задержки роста, дифференциации, развития, а также активируется при употреблении некоторых препаратов[32].
Регуляция стабильности мРНК
Судьба мРНК является другой ключевой точкой в посттранскрипционной регуляции экспрессии генов, так как в отсутствие разрушения определённых мРНК их число будет расти, а значит, увеличится количество кодируемого ими белка, что может повлиять на экспрессию тех или иных генов. Было предложено несколько возможных механизмов разрушения мРНК: её деградация может запускаться укорочением или отрывом 3′-поли(А)-хвоста или 5′-кэпа[33]. Судьба мРНК в основном регулируется цис-регуляторными элементами, расположенными в 3′-UTR, например, AU-богатыми элементами (AREs[en]*), которые запускают распад мРНК под влиянием различных внутри- и внеклеточных сигналов. По имеющимся экспериментальным данным AREs разделили на 3 класса: для членов I и II класса характерно наличие множества копий пентануклеотида AUUUA, чего нет у представителей III класса[34]. AREs I класса контролируют цитоплазматическое деаденилирование путём деградации всего поли(А)-хвоста с одинаковой скоростью у всех транскриптов с образованием сначала промежуточных соединений с поли(А)-хвостом в 30—60 нуклеотидов, которые потом полностью деградируют. Такие элементы обнаруживаются в основном в мРНК, кодирующих ядерные факторы транскрипции, например, c-Fos и c-Myc (продукты генов «быстрого ответа»), а также мРНК, кодирующих некоторые цитокины, например, интерлейкины 4 и 6. Структурной характеристикой AREs I класса является наличие одной или нескольких копий пентануклеотида AUUUA после U-богатого участка. AREs II класса управляют асинхронным цитоплазматическим деаденилированием (то есть поли(А)-хвост различных транскриптов разрушается с различной скоростью), в результате которого образуется мРНК без поли(А)-хвоста. В число мРНК, содержащих такие элементы, входят мРНК цитокинов GM-CSF, интерлейкин 2, фактор некроза опухоли α (TNF-α), интерферон-α. Структурной особенностью AREs второго класса является наличие тандемных повторов пентануклеотида AUUUA, а AU-богатый участок располагается до этих повторов. У AREs III класса отсутствует пентануклеотид AUUUA и есть только U-богатый участок. Такой элемент есть, например, у мРНК, кодирующей c-Jun. Кинетика деградации мРНК в этом случае схожа с таковой у AREs I[3].
Деградация мРНК может также осуществляться за счёт эндонуклеазной активности, причём такой механизм зависим и от деаденилирования, и декэпирования. Этот механизм был обнаружен у мРНК, кодирующих трансферриновый рецептор[en]. Деградация этих мРНК включает эндонуклеазное разрезание 3′-UTR, причём промежуточным этапом является распознавание IRE, а регуляция определяется уровнем внутриклеточного железа[35].
Инициаторные кодоны в 5′-UTR и uORF также могут играть роль в особом механизме распада бессмысленных (англ. nonsense) («бракованных») мРНК — NMD[en]* (англ. nonsense-mediated mRNA decay). Сигналом, запускающим этот путь, является бессмысленный кодон, вслед за которым идёт соединение между двумя экзонами, образовавшееся при сплайсинге — комплекс соединения экзонов, или EJC[en] (англ. Exon junction complex)[36] (наличие такого соединения отличает преждевременный терминаторный кодон от основного, так как стоп-кодон и 3′-UTR располагаются после последнего экзона). Соединения экзонов распознаются благодаря маркерным белкам, присоединяющимся к непроцессированному транскрипту ещё в ядре и остающимся связанными с ним после процессинга и перехода мРНК в цитоплазму[37]. В случае мРНК дикого типа (то есть «небракованных») аппарат трансляции убирает маркерный белок для предотвращения деградации транскрипта. Если же рибосома встречает преждевременный стоп-кодон или если в транскрипте присутствуют uORF, она распадается, и меченная маркерными белками дефектная мРНК вовлекается в NMD[38]. У дрожжей Saccharomyces cerevisiae (у них имеется второй сигнал, запускающий NMD — нижестоящие экзонные элементы (англ. downstream exonic element (DSE)) мРНК, содержащие функционально активные uORF, например, кодирующие GCN4 и YAP1, не деградируют по пути NMD. Дело в том, что между uORF и кодирующей последовательностью располагаются мРНК-специфические стабилизирующие последовательности, предотвращающие активацию NMD за счёт взаимодействия с РНК-связывающей убиквитин—лигазой Pub1[39].
uORF могут регулировать стабильность мРНК и независимо от NMD. В 5′-UTR мРНК гена YAP2 S. cerevisiae содержится 2 uORF, которые подавляют сканирование транскрипта рибосомой и способствуют распаду мРНК[40]. Дестабилизирующий эффект зависит от окружения терминаторного кодона, которое регулирует эффективность трансляции и стабильность мРНК.
Несколько исследований дают основание предположить, что многие гетерогенные ядерные рибонуклеопротеины[en] (англ. heterogeneous nuclear ribonucleoproteins (hnRNPs)) функционируют не только в ядре, но также контролируют судьбу мРНК в цитоплазме[41], регулируют трансляцию, стабильность мРНК и её локализацию в цитоплазме[38]. Примером может служить белок-предшественник амилоидов (англ. amyloid precursor protein (APP)). Повышение содержания APP является важным фактором развития болезни Альцгеймера. Стабильность мРНК APP зависит от высококонсервативного 29-нуклеотидного элемента, расположенного в 3′-UTR и взаимодействующего с различными РНК-связывающими цитоплазматическими белками[42].
Контроль внутриклеточной локализации мРНК
Контроль экспрессии генов на посттранскрипционном уровне, осуществляемый нетранслируемыми областями, особенно важен в период развития. Асимметричное расположение в клетке некоторых мРНК приводит к асимметричному расположению кодируемых ими белков. Это — наиболее удобный механизм локализации белков, так как одна мРНК может служить матрицей для нескольких кругов трансляции. Во многих случаях мРНК располагаются в рибонуклеопротеиновых комплексах вместе с белками трансляционного аппарата, тем самым гарантируя необходимую эффективность трансляции[3].
Существуют 3 основных механизма асимметричного расположения мРНК:
- активный направленный транспорт, в котором задействован функциональный цитоскелет и моторные белки, взаимодействующие с мРНК;
- локальная стабилизация транскриптов;
- диффузия мРНК, определяемая её локальным окружением[3].
мРНК основного белка миелина (англ. Myelin basic protein (MBP)) доставляется в отростки олигодендроцитов, образующих миелиновую обкладку аксонов ЦНС, через активный направленный транспорт. У мыши для транспорта и локализации мРНК служат особые сигнальные последовательности, располагающиеся в 3′-UTR: РНК-транспортный сигнал (длиной 21 нуклеотид), а также дополнительный элемент — регион РНК-локализации[43].
Многие примеры локальной стабилизации транскриптов обнаружены в ранних стадиях развития дрозофилы. Так, транскрипты, кодирующие РНК-связывающий белок Nanos и белок теплового шока Hsp83 деградируются везде, кроме цитоплазмы на заднем полюсе эмбриона. Различные цис-регуляторные элементы, располагающиеся в 3′-UTR соответствующих мРНК, отвечают как за деградацию этих мРНК по всему зародыщу, так и за их стабилизацию на заднем конце зародыша[44].
Явление диффузии мРНК, определяемой окружением, хорошо демонстрирует мРНК белка Bicoid у дрозофилы. Элементы, осуществляющие ключевой этап в этом процессе — заякоривание транскрипта, не полностью описаны, но один из участвующих в этом белок — Staufen[en] — является дцРНК-связывающим белком, необходимым для остановки Bicoid на переднем конце зародыша[45].
Во всех приведённых выше примерах локализация регулировалась цис-регуляторными элементами, расположенными в 3′-UTR, но известны и такие элементы, расположенные в 5′-UTR и даже кодирующей области. Такие элементы известны как мРНК-архивирующие коды (англ. mRNA zip codes), они взаимодействуют с соответствующими связывающими белками (англ. zip-code-binding proteins), например, уже упоминавшимся Staufen. У архивирующих кодов отсутствует какое-либо сходство в первичной и вторичной структуре. Они могут иметь сложную (комплексную) вторичную и третичную структуру, в которой первичная структура (последовательность нуклеотидов) не так важна, как пространственная структура[46], а могут, напротив, быть короткими нуклеотидными последовательностями[47], иногда входящими в повторяющиеся элементы (например, в случае транскрипта Vg1[en] у лягушки Xenopus[48]).
Ремоделирование UTR
Альтернативный сплайсинг является важнейшим путём образования из одного исходного транскрипта различных мРНК, кодирующих одинаковые или различные белки. При этом, помимо длинных белоккодирующих мРНК, могут образовываться и некодирующие РНК. Разрезанная мРНК может подвергнуться процессу рекэпирования с образованием мРНК с укороченной 5′-нетранслируемой областью или же кодирующая лишь фрагмент исходного белка. Кроме того, известно, что образовавшиеся в ходе альтернативного сплайсинга 3′-UTR-фрагменты могут начать функционировать как транс-регуляторные некодирующие РНК независимо от основной РНК[49].
Взаимодействие 5′-UTR и 3′-UTR
 Циркуляризация (замыкание в петлю) мРНК
Циркуляризация (замыкание в петлю) мРНК
Известно, что мРНК способна замыкаться в петлю (циркуляризация) за счёт взаимодействия специфических белков, связывающихся с поли(А)-хвостом, способствующих связыванию фактора eIF4F с кэпом. В результате мРНК приобретает замкнутую форму, стимулируется инициация трансляции и повышается эффективность трансляции. Однако в некоторых случаях 5′-UTR и 3′-UTR одной и той же мРНК могут связываться друг с другом комплементарно. Так, у мРНК человеческого гена, кодирующего p53, имеются участки в 5′-UTR и 3′-UTR, комплементарные друг другу. Связываясь друг с другом и с трансляционным фактором RPL26[en], они тем самым способствуют повышению эффективности трансляции, что является одной из причин быстрого накопления белка р53 в ответ на повреждения ДНК[50].
Анализ мРНК различных генов человека показал, что в 5′-UTR присутствует мотив, специфически взаимодействующий с 3′-концами микроРНК, при этом во многих таких мРНК на 5′-конце имеется сайт, комплиментарный 3′-UTR. Дальнейшие исследования показали, что связывание 5′-UTR с микроРНК облегчает связь 5′-конца мРНК с 3′-концом, и мРНК, активность которых значительно определяется микроРНК, имеют предсказуемые сайты связывания на обеих UTR. Такие мРНК получили название miBridge. Далее было установлено, что утрата этих сайтов связывания уменьшала репрессию трансляции транскрипта, управляемую микроРНК. Так было выяснено, что сайты связывания UTR друг с другом необходимы для подавления трансляции мРНК. Это свидетельствует о том, что комплиментарное взаимодействие 5′-UTR и 3′-UTR необходимо для точной регуляции экспрессии генов[51].
UTR прокариот и вирусов
Бактерии
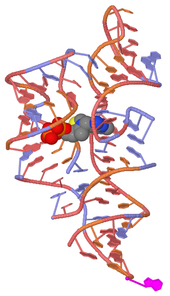 3D-структура TPP-рибопереключателя[en][52]
3D-структура TPP-рибопереключателя[en][52]
В мРНК бактерий также имеются 5′- и 3′-нетранслируемые области[53][54]. Длина 5′-UTR бактерий значительно меньше таковой у эукариот и составляет обычно 3—10 нуклеотидов. Например, длина 5′-UTR транскрипта лактозного оперона Escherichia coli составляет лишь 7 нуклеотидов[55]. В 5′-UTR бактерий локализована последовательность Шайна — Дальгарно (AGGAGG)[56], служащая для связывания рибосомы и отделённая спейсером от стартового кодона AUG. Хотя 5′-UTR бактерий и эукариот различны, было показано, что добавление нуклеотидов СС в спейсер мРНК гена Ner бактериофага Mu, хорошо экспрессирующегося в клетках Escherichia coli и Streptomyces, привело к успешной экспрессии этого гена в клетках ретикулоцитов кролика[57].
Элементы вторичной структуры, локализованные в 5′-UTR, как правило, оказывают подавляющее действие на трансляцию[58]. В частности, именно в 5′-UTR обычно располагаются аттенюаторы[en] — элементы оперонов, вызывающие преждевременную терминацию трансляции[59] (наиболее известным примером аттенюации является экспрессия триптофанового оперона).
Кроме того, в 5′-UTR бактерий располагается большая часть рибопереключателей[60] — регуляторных элементов мРНК, способных связываться с малыми молекулами?!, что приводит к изменению эффективности образования белка, кодируемого этой мРНК[61].
В отличие от эукариот, длинные 3′-UTR редки у бактерий и слабо изучены. Тем не менее, известно, что у некоторых бактерий, в частности, Salmonella enterica?!, имеются мРНК с длинными 3′-UTR, похожими на эукариотические (у S. enterica это мРНК hilD). Предполагается, что 3′-UTR hilD выполняют различные функции, в частности, влияют на обращение своих мРНК, поскольку делеция этих областей вызывала увеличение количества соответствующих мРНК[62].
Археи
Нетранслируемые области имеются и в мРНК многих архей. В частности, в 5′- и 3′-UTR мРНК метаногенной археи Methanocaldococcus jannaschii[en] (как и у других представителей порядков Methanopyrales[en]* и Methanococcales) локализован элемент SECIS, ответственный за вставку аминокислоты селеноцистеина в полипептидную цепь[63].
Установлено, что мРНК большинства галоархей, а также Pyrobaculum[en] и Sulfolobus[en] лишены выраженной 5′-UTR, но у мРНК архей-метаногенов имеются длинные 5′-UTR. В связи с этим предполагается, что механизм инициации трансляции метаногенных архей может быть отличен от такового у остальных представителей этого домена[58]. Тем не менее, в мРНК галоархей имеются 3′-UTR и их 3′-концы не подвергаются посттранскрипционной модификации. Удивительным является тот факт, что в тех транскриптах галоархей, у которых есть 5′-UTR, отсутствует последовательность Шайна — Дальгарно. Длина же 3′-UTR галоархей составляла от 20 до 80 нуклеотидов; никаких консервативных структурных мотивов и последовательностей, кроме пента-U-нуклеотида в области терминации трансляции, выявлено не было[64].
Для мРНК архей описаны рибопререключатели, в том числе TPP-рибопереключатели[en] (связываются с тиаминпирофосфатом (TPP)), которые располагаются в 5′-UTR (подобные рибопереключатели имеются также у бактерий и эукариот)[65].
Вирусы
 РНК—геном полиовируса. В 5′-UTR находится IRES.
РНК—геном полиовируса. В 5′-UTR находится IRES.
У многих вирусов инициация трансляции происходит по кэп-независимому механизму и осуществляется через уже упоминавшиеся элементы IRES, локализованные в 5′-UTR[66]. Например, так происходит у ВИЧ, вирусов гепатита А и С[67]. Такой механизм инициации трансляции удобен тем, что в его случае нет необходимости в сборке пре-инициаторного белкового комплекса, и вирус может быстро размножаться[55].
У вирусов существует и другой кэп-независимый механизм инициации трансляции, не связанный с IRES. Такой механизм имеется у многих вирусов растений[en]*. В этом случае имеется особый кэп-независимый трансляционный элемент (англ. cap-independent translation element (CITE)), расположенный в 3′-UTR. Нередко CITE связывает факторы трансляции, например, комплекс eIF4F, и затем комплементарно взаимодействует с 5′-концом, доставляя факторы инициации трансляции к месту её начала[68].
У вирусов, геном которых представлен одноцепочечной молекулой РНК положительной полярности[en], 3′-UTR не только оказывает влияние на трансляцию, но также задействована в репликации: именно с неё начинается репликация вирусного генома[69].
Вирус кори (род Morbillivirus?! семейства Paramyxoviridae) имеет геном, представленный одноцепочечной молекулой РНК отрицательной полярности. Для его генов М и F был установлен интересный механизм. мРНК этих генов имеют длинные UTR, на их долю приходится ~6,4 % всей мРНК. Хотя эти гены непосредственно не участвуют в репликации, 3′-UTR мРНК гена М увеличивает скорость накопления белка М и тем самым запускает репликацию генома. В то же время 5′-UTR мРНК гена F снижает образование белка F и тем самым подавляет репликацию[70].
Клиническое значение
Так как нетранслируемые области играют важнейшие роли в регуляции экспрессии генов, различные изменения, затрагивающие эти области, нередко ведут к появлению болезненных состояний, таких как наследственная тромбоцитемия[en], рак молочной железы, синдром ломкой Х-хромосомы, биполярное аффективное расстройство, болезнь Альцгеймера и других[71]. В представленных ниже схемах показаны связи между мутациями, затрагивающими тот или иной функциональный элемент 3′-UTR и 5′-UTR, и различными заболеваниями.
Мутации UTR и заболевания человека
 Мутации, затрагивающие 5′-UTR, и связанные с ними заболевания
Мутации, затрагивающие 5′-UTR, и связанные с ними заболевания Мутации, затрагивающие 3′-UTR, и связанные с ними заболевания
Мутации, затрагивающие 3′-UTR, и связанные с ними заболевания
Примечания
- ↑ Коничев, Севастьянова, 2012, с. 108.
- ↑ Barrett et. al., 2013, p. 9.
- ↑ 1 2 3 4 5 6 7 8 9 Flavio Mignone, Carmela Gissi, Sabino Liuni, Graziano Pesole. Untranslated regions of mRNAs // Genome Biol.. — 2002. — Т. 3, № 3.
- ↑ Шаблон:Ссылка
- ↑ Rhind, Nicholas; Chen, Zehua; Yassour, Moran; Thompson, Dawn A.; Haas, Brian J.; Habib, Naomi; Wapinski, Ilan; Roy, Sushmita; Lin, Michael F.; Heiman, David I.; Young, Sarah K.; Furuya, Kanji; Guo, Yabin; Pidoux, Alison; Chen, Huei Mei; Robbertse, Barbara; Goldberg, Jonathan M.; Aoki, Keita; Bayne, Elizabeth H.; Berlin, Aaron M.; Desjardins, Christopher A.; Dobbs, Edward; Dukaj, Livio; Fan, Lin; Fitzgerald, Michael G.; French, Courtney; Gujja, Sharvari; Hansen, Klavs; Keifenheim, Dan; Levin, Joshua Z. (2011). “Comparative Functional Genomics of the Fission Yeasts”. Science. 332 (6032): 930—6. DOI:10.1126/science.1203357. PMC 3131103. PMID 21511999.
- ↑ Pesole G, Mignone F, Gissi C, Grillo G, Licciulli F, Liuni S. Structural and functional features of eukaryotic mRNA untranslated regions // Gene. — 2001. — Т. 276, № 1—2. — С. 73—81.
- ↑ Hughes M. J., Andrews D. W. A single nucleotide is a sufficient 5′ untranslated region for translation in an eukaryotic in vitro system. // FEBS Lett.. — 1997. — Т. 414, № 1. — С. 19—22.
- ↑ Grabowski P. J., Black D. L. Alternative RNA splicing in the nervous system // Prog Neurobiol.. — 2001. — Т. 65, № 3. — С. 289—308.
- ↑ Pesole G, Liuni S, Grillo G, Saccone C. Structural and compositional features of untranslated regions of eukaryotic mRNAs. // Gene. — 1997. — Т. 205, № 1—2. — С. 95—102.
- ↑ Pesole G., Bernardi G., Saccone C. Isochore specificity of AUG initiator context of human genes. // FEBS Lett.. — 1999. — Т. 464, № 1—2. — С. 60—62.
- ↑ Duret L., Mouchiroud D., Gautier C. Statistical analysis of vertebrate sequences reveals that long genes are scarce in GC-rich isochores. // J Mol Evol.. — 1995. — Т. 40, № 3. — С. 308—317.
- ↑ Jansen R. P. mRNA localization: message on the move. // Nat Rev Mol Cell Biol.. — 2001. — Т. 2, № 4. — С. 247—256.
- ↑ Bashirullah A., Cooperstock R. L., Lipshitz H. D. Spatial and temporal control of RNA stability. // Proc Natl Acad Sci USA.. — 2001. — Т. 98, № 13. — С. 7025—7028.
- ↑ van der Velden A. W., Thomas A. A. The role of the 5′ untranslated region of an mRNA in translation regulation during development. // Int J Biochem Cell Biol.. — 1999. — Т. 31, № 1. — С. 87—106.
- ↑ Walczak R., Westhof E., Carbon P., Krol A. A novel RNA structural motif in the selenocysteine insertion element of eukaryotic selenoprotein mRNAs. // RNA. — 1996. — Т. 2, № 4. — С. 367—379.
- ↑ Conne B., Stutz A., Vassalli J. D. The 3′ untranslated region of messenger RNA: A molecular ‘hotspot’ for pathology? // Nat Med.. — 2000. — Т. 6, № 6. — С. 637—641.
- ↑ Sweeney R., Fan Q., Yao M. C. Antisense ribosomes: rRNA as a vehicle for antisense RNAs. // Proc Natl Acad Sci USA. — 1996. — Т. 93, № 16. — С. 8518—8523.
- ↑ Timchenko L. T. Myotonic dystrophy: the role of RNA CUG triplet repeats. // Am J Hum Genet.. — 1999. — Т. 64, № 2. — С. 360—364.
- ↑ Anderson L., Seilhamer J. A comparison of selected mRNA and protein abundances in human liver. // Electrophoresis. — 1997. — Т. 18, № 3—4. — С. 533—537.
- ↑ Kozak M. An analysis of 5′-noncoding sequences from 699 vertebrate messenger RNAs. // Nucleic Acids Res.. — 1987. — Т. 15, № 20. — С. 8125—8148.
- ↑ Maitra U., Stringer E. A., Chaudhuri A. Initiation factors in protein biosynthesis. // Annu Rev Biochem.. — 1982. — Т. 51. — С. 869—900.
- ↑ Michel Y. M., Poncet D., Piron M., Kean K. M., Borman A. M. Cap-Poly(A) synergy in mammalian cell-free extracts. Investigation of the requirements for poly(A)-mediated stimulation of translation initiation. // J Biol Chem.. — 2000. — Т. 275, № 41. — С. 32268—76.
- ↑ Xiong W., Hsieh C. C., Kurtz A. J., Rabek J. P., Papaconstantinou J. Regulation of CCAAT/enhancer-binding protein-beta isoform synthesis by alternative translational initiation at multiple AUG start sites. // Nucleic Acids Res.. — 2001. — Т. 29, № 14. — С. 3087—98.
- ↑ Rogozin I. B., Kochetov A. V., Kondrashov F. A., Koonin E. V., Milanesi L. Presence of ATG triplets in 5′ untranslated regions of eukaryotic cDNAs correlates with a ‘weak’ context of the start codon. // Bioinformatics. — 2001. — Т. 17, № 10. — С. 890—900.
- ↑ Cassan M., Rousset J. P. UAG readthrough in mammalian cells: effect of upstream and downstream stop codon contexts reveal different signals. // BMC Mol Biol.. — 2001. — Т. 2. — С. 3.
- ↑ Luukkonen B. G., Tan W., Schwartz S. Efficiency of reinitiation of translation on human immunodeficiency virus type 1 mRNAs is determined by the length of the upstream open reading frame and by intercistronic distance. // J Virol.. — 1995. — Т. 69, № 7. — С. 4086—94.
- ↑ Vilela C., Ramirez C. V., Linz B., Rodrigues-Pousada C., McCarthy J. E. Post-termination ribosome interactions with the 5’UTR modulate yeast mRNA stability. // EMBO J.. — 1999. — Т. 18, № 11. — С. 3139—52.
- ↑ Svitkin Y. V., Pause A., Haghighat A., Pyronnet S., Witherell G., Belsham G. J., Sonenberg N. The requirement for eukaryotic initiation factor 4A (elF4A) in translation is in direct proportion to the degree of mRNA 5′ secondary structure. // RNA. — 2001. — Т. 7, № 3. — С. 382—94.
- ↑ Pelletier J., Kaplan G., Racaniello V. R., Sonenberg N. Cap-independent translation of poliovirus mRNA is conferred by sequence elements within the 5′ noncoding region. // Mol Cell Biol.. — 1988. — Т. 8, № 3. — С. 1103—12.
- ↑ Le S. Y., Maizel J. V. A common RNA structural motif involved in the internal initiation of translation of cellular mRNAs. // Nucleic Acids Res.. — 1997. — Т. 25, № 2. — С. 362—69.
- ↑ Chappell S. A., Edelman G. M., Mauro V. P. A 9-nt segment of a cellular mRNA can function as an internal ribosome entry site (IRES) and when present in linked multiple copies greatly enhances IRES activity. // Proc Natl Acad Sci USA.. — 2000. — Т. 97, № 4. — С. 1536—41.
- ↑ Shama S., Meyuhas O. The translational cis-regulatory element of mammalian ribosomal protein mRNAs is recognized by the plant translational apparatus. // Eur J Biochem.. — 1996. — Т. 236, № 2. — С. 383—8.
- ↑ Brown C. E., Sachs A. B. Poly(A) tail length control in Saccharomyces cerevisiae occurs by message-specific deadenylation. // Mol Cell Biol.. — 1998. — Т. 18, № 11. — С. 6548—59.
- ↑ Peng S. S., Chen C. Y., Shyu A. B. Functional characterization of a non-AUUUA AU-rich element from the c-jun proto-oncogene mRNA: evidence for a novel class of AU-rich elements. // Mol Cell Biol.. — 1996. — Т. 16, № 4. — С. 1490—9.
- ↑ Hentze M. W., Kühn L. C. Molecular control of vertebrate iron metabolism: mRNA-based regulatory circuits operated by iron, nitric oxide, and oxidative stress. // Proc Natl Acad Sci USA.. — 1996. — Т. 93, № 16. — С. 8175—82.
- ↑ Hentze M. W., Kulozik A. E. A perfect message: RNA surveillance and nonsense-mediated decay. // Cell.. — 1999. — Т. 96, № 3. — С. 307—10.
- ↑ Kataoka N., Yong J., Kim V. N., Velazquez F., Perkinson R. A., Wang F., Dreyfuss G. Pre-mRNA splicing imprints mRNA in the nucleus with a novel RNA-binding protein that persists in the cytoplasm. // Mol Cell.. — 2000. — Т. 6, № 3. — С. 673—82.
- ↑ 1 2 Shyu A. B., Wilkinson M. F. The double lives of shuttling mRNA binding proteins. // Cell.. — 2000. — Т. 102, № 2. — С. 135—8.
- ↑ Ruiz-Echevarría M. J., Peltz S. W. The RNA binding protein Pub1 modulates the stability of transcripts containing upstream open reading frames. // Cell.. — 2000. — Т. 101, № 7. — С. 741—51.
- ↑ Vilela C., Ramirez C. V., Linz B., Rodrigues-Pousada C., McCarthy J. E. Post-termination ribosome interactions with the 5’UTR modulate yeast mRNA stability. // EMBO J.. — 1999. — Т. 18, № 11. — С. 3139—52.
- ↑ Xu N., Chen C. Y., Shyu A. B. Versatile role for hnRNP D isoforms in the differential regulation of cytoplasmic mRNA turnover. // Mol Cell Biol.. — 2001. — Т. 21, № 20. — С. 6960—71.
- ↑ Zaidi S. H., Malter J. S. Amyloid precursor protein mRNA stability is controlled by a 29-base element in the 3′-untranslated region. // J Biol Chem.. — 1994. — Т. 269, № 39. — С. 24007—13.
- ↑ Ainger K., Avossa D., Diana A. S., Barry C., Barbarese E., Carson J. H. Transport and localization elements in myelin basic protein mRNA. // J Cell Biol.. — 1997. — Т. 138, № 5. — С. 1077—87.
- ↑ Bashirullah A., Cooperstock R. L., Lipshitz H. D. Spatial and temporal control of RNA stability. // Proc Natl Acad Sci USA.. — 2001. — Т. 98, № 13. — С. 7025—8.
- ↑ St Johnston D., Beuchle D., Nüsslein-Volhard C. Staufen, a gene required to localize maternal RNAs in the Drosophila egg. // Cell.. — 1991. — Т. 66, № 1. — С. 51—63.
- ↑ Macdonald P. M., Kerr K., Smith J. L., Leask A. RNA regulatory element BLE1 directs the early steps of bicoid mRNA localization. // Development. — 1993. — Т. 118, № 4. — С. 1233—43.
- ↑ Chan A. P., Kloc M., Etkin L. D. fatvg encodes a new localized RNA that uses a 25-nucleotide element (FVLE1) to localize to the vegetal cortex of Xenopus oocytes. // Development. — 1999. — Т. 126, № 22. — С. 4943—53.
- ↑ Mowry K. L., Melton D. A. Vegetal messenger RNA localization directed by a 340-nt RNA sequence element in Xenopus oocytes. // Science. — 1992. — Т. 255, № 5047. — С. 991—4.
- ↑ Flavio Mignone, Graziano Pesole. mRNA Untranslated Regions (UTRs) // eLS. — С. 1—5. — doi:10.1002/9780470015902.a0005009.pub2.
- ↑ Barrett et. al., 2013, с. 32.
- ↑ Barrett et. al., 2013, с. 32—33.
- ↑ Edwards TE, Ferré-D’Amaré AR (2006). “Crystal structures of the thi-box riboswitch bound to thiamine pyrophosphate analogs reveal adaptive RNA-small molecule recognition”. Structure. 14 (9): 1459—68. DOI:10.1016/j.str.2006.07.008. PMID 16962976.
- ↑ Льюин Б. Гены. — БИНОМ, 2012. — С. 144. — 896 с. — ISBN 978-5-94774-793-5.
- ↑ Н. В. Равин, С. В. Шестаков. Геном прокариот // Вавиловский журнал генетики и селекции. — 2013. — Т. 17, № 4/2. — С. 972—984.
- ↑ 1 2 Brown, T.A. Genomes 3. — New York, New York : Garland Science Publishing, 2007. — P. 397. — ISBN 0 8153 4138 5.
- ↑ John W. Pelley. Elsevier’s Integrated Review Biochemistry. — 2nd Edition. — 2012. — ISBN 978-0-32307-446-9.
- ↑ A 5′ untranslated region which directs accurate and robust translation by prokaryotic and mammalian ribosomes.
- ↑ 1 2 Jian Zhang. Gene expression in Archaea: Studies of transcriptional promoters, messenger RNA processing, and five prime untranslated regions in Methanocaldococcus jannashchii. — 2009.
- ↑ Magali Naville, Daniel Gautheret. Transcription attenuation in bacteria: theme and variations // Brief Funct Genomic Proteomic. — 2009. — Т. 8. — С. 482—492.
- ↑ Шаблон:Ссылка
- ↑ Nudler E, Mironov AS (2004). “The riboswitch control of bacterial metabolism”. Trends Biochem Sci. 29 (1): 11—7. DOI:10.1016/j.tibs.2003.11.004. PMID 14729327.
- ↑ Javier López-Garrido, Elena Puerta-Fernández, Josep Casadesús. A eukaryotic-like 3′ untranslated region in Salmonella enterica hilD mRNA // Nucl. Acids Res.. — 2014. — ISSN 1362-4962. — doi:10.1093/nar/gku222.
- ↑ R. Wilting, S. Schorling, B. C. Persson, A. Bock. Selenoprotein Synthesis in Archaea: Identification of an mRNA Element of Methanococcus jannaschii Probably Directing Selenocysteine Insertion // J. Mol. Biol.. — 1997. — Т. 266. — С. 637—641.
- ↑ Brenneis M., Hering O., Lange C., Soppa J. Experimental characterization of Cis-acting elements important for translation and transcription in halophilic archaea. // PLoS Genet.. — 2007. — Т. 3, № 12. — doi:10.1371/journal.pgen.0030229.
- ↑ Kosuke Fujishima, Akio Kanai. Diversity, Function, and Processing of Archaeal Non-Coding RNAs // Sakura Y. Kato Archaea: Structure, Habitats and Ecological Significance. — Nova Science Publishers, Inc., 2011. — С. 69—94. — ISBN 978-1-61761-932-8.
- ↑ Thompson, Sunnie R. (2012). “Tricks an IRES uses to enslave ribosomes”. Trends in Microbiology. 20 (11): 558—66. DOI:10.1016/j.tim.2012.08.002. PMC 3479354. PMID 22944245.
- ↑ Jeffrey S. Kieft. Viral IRES RNA structures and ribosome interactions // Trends in Biochemical Sciences. — 2008. — Т. 33, № 6. — С. 274—283. — doi:10.1016/j.tibs.2008.04.007.
- ↑ Qiuling Fan, Krzysztof Treder, W Allen Miller. Untranslated regions of diverse plant viral RNAs vary greatly in translation enhancement efficiency // BMC Biotechnology. — 2012. — Т. 12, № 22. — doi:10.1186/1472-6750-12-22.
- ↑ Dreher T. W. FUNCTIONS OF THE 3′-UNTRANSLATED REGIONS OF POSITIVE STRAND RNA VIRAL GENOMES // Annu Rev Phytopathol.. — 1999. — Т. 37. — С. 151—174.
- ↑ Makoto Takeda, Shinji Ohno, Fumio Seki, Yuichiro Nakatsu, Maino Tahara, Yusuke Yanagi. Long Untranslated Regions of the Measles Virus M and F Genes Control Virus Replication and Cytopathogenicity // J. Virol.. — 2005. — Т. 79, № 22. — С. 14346—14354. — doi:10.1128/JVI.79.22.14346-14354.2005.
- ↑ Sangeeta Chatterjee, Jayanta K. Pal. Role of 5- and 3-untranslated regions of mRNAs in human diseases // Biol. Cell. — 2009. — С. 251—262. — doi:10.1042/BC20080104.
Литература
- Коничев А. С., Севастьянова Г. А. Молекулярная биология. — Издательский центр «Академия», 2012. — 400 с. — ISBN 978-5-7695-9147-1.
- Lucy W. Barrett, Sue Fletcher, Steve D. Wilton. Untranslated Gene Regions and Other Non-coding Elements. — SpringerBriefs in Biochemistry and Molecular Biology, 2013. — 57 p. — ISBN 978-3-0348-0679-4.
Ссылки
- Шаблон:Ссылка (англ.)
| Эта статья входит в число хороших статей и является кандидатом в избранные с 13 августа 2014. |


